Hvad opmuntrer os til at spise? Faktorer, der starter og stopper indtagelse

- 1887
- 468
- Taylor Mitchell DDS
Flere faktorer påvirker, hvilken tid vi spiser, det beløb, vi spiser, og når vi holder op med at gøre det.
Indhold
Skift- Hvad der begynder at spise opførsel?
- Hvad til opførsel af at spise? (Mættethedssignaler)
- Kort -term metthedssignaler
- Lange -term metthedssignaler
- Leptinfunktion
- Hvor handler den frigjorte leptin?
- Insulinfunktion
Hvad der begynder at spise opførsel?
Vi har en tendens til at overveje, at mad kun er vigtig for fysiologiske processer. Det vil sige, vi spiser, når vi har brug for kalorier.
Men vi må huske på det Mad er en relativt ineffektiv måde at hurtigt få blodkalorier på. For at øge blodnæringsniveauerne skal mad forarbejdes, fordøjes i maven, skal passere tarmen og skal absorberes i blod.
Heldigvis under normale forhold er det ikke hyppigt, at blodbrændstofniveauer er under dem, der er nødvendige for at imødekomme behovene i de forskellige væv. Og derfor, Vi begynder at spise, når vi stadig har vigtige mængder energi til rådighed.
Madadfærd er meget påvirket af sociale og kulturelle faktorer. Mange gange spiser vi for vaner eller ved virkning af forskellige stimuli i miljøet, såsom visionen eller aromaen af mad, et ur, der indikerer, at det spiser tid osv.
Mange undersøgelser har vist, at spiseadfærd kan konditioneres klassisk, og derfor kan enhver stimulus, der har været forbundet med madindtagelse, forårsage spiseadfærd.
Men indtagelse afhænger også af metaboliske faktorer.
Hvis vi springer måltider over, vil vi være mere sultne, og dette gennemgår helt sikkert eksistensen af fysiologiske signaler, der indikerer faldet i næringsstoffer fra vores lange reserver. Så, Brugen af lange reserver kan give et indikatorsignal, der spiser tid.
Det ser ud til at være tydeligt, at følelsen af sult er omvendt relateret til mængden af næringsstoffer, der er overdrevent indtaget i den forrige mad.
Hjernen reagerer på to typer appetitsignaler:
- Kort -term signal: De bestemmes af tilgængeligheden af blodnæringsstoffer og detekteres af lever- og hjernereceptorer.
- Langt -term signal: De stammer fra fedtvævet, der indeholder de lange reserver.
Når reservaterne er fulde, er et peptidhormon, der har en hæmmende virkning på hjernemekanismerne, der kontrollerer at spise opførsel. Når niveauet for dette hormon er højt, bliver hjernen mindre følsom over for sultskilte På kort sigt rapporterer denne tilgængelighed af næringsstoffer, der producerer et fald i indtagelse.
Før en langvarig fasteperiode falder lange reserver for reserver, og fedtceller mindsker frigivelsen af dette hormon, At forårsage hjernemekanismer, der kontrollerer spiseopførsel, bliver mere følsomme over for korte sulttegn.

Hvad til opførsel af at spise? (Mættethedssignaler)
Mættethedsskiltene er ikke nødvendigvis de samme, der begynder at spise opførsel. Vi holder ikke op med at spise, så vi har genvundet de forskellige næringsstoffer, men vi gør det længe før dette sker.
Der er to hovedkilder til metthedssignaler:
- Kort -term -signaler: De er relateret til de umiddelbare konsekvenser af indtagelse af et specifikt måltid og antyder cephaliske, gastriske, tarm- og leverfaktorer. Det er tegn, der kommer fra de umiddelbare konsekvenser af mad. I disse signaler kan de involveres receptorer placeret i ansigtet (som giver information om smag, lugt, tekstur af mad), i maven, tolvfingertarmen og leveren. Disse signaler kan udgøre indikatorer for, at maden er blevet absorberet og fordøjes.
- Lange -term -signaler: De stammer fra fedtvævet og tillader at opretholde kropsvægt. Disse signaler kontrollerer kalorier ved at modulere følsomheden af de hjernemekanismer, der er involveret i indtagelsen.
Indtagelse af kontrol indebærer en interaktion mellem korte signaler og lang sigt på lang sigt. Hvis en person ikke har spist nok til at bevare deres vægt, vil det være mindre følsomt over for mættethedssignaler leveret af mad (korte -termiske signaler) og derfor har en tendens til at spise mere. Hvis en person har spist i overskud og har vundet vægt, vil det være mere følsomt over for korte mættethedssignaler leveret af den samme mad.
 Centralnervesystem (CNS): Struktur, funktioner og sygdomme
Centralnervesystem (CNS): Struktur, funktioner og sygdomme Kort -term metthedssignaler
Cephaliske faktorer henviser til Tegn relateret til smag, lugt og tekstur af mad. Disse foregribende faktorer virker uvæsentlige, hvis vi sammenligner dem med andre signaler fra mave, tarme eller stadier efter fødevareabsorption.
For eksempel, når en gastrisk fistel implanteres til en rotte, der forhindrer mad i at nå maven, spiser dyret kontinuerligt uden at vise tegn på metthed. Det ser ud til, at mad i det mindste skal ankomme i maven for at udløse tegn på metthed.
Det faktum, at vi holder op med at spise længe før fordøjelse og madabsorption finder sted i tarmen ser ud til at indikere, at tegn, der stammer fra maven, kunne være vigtige i mættethedsmekanismer.
Distensionen af maven, som et resultat af volumenforøgelsen, udgør et metthedssignal.
I mavevæggene er der receptorer, der øger deres aktivitet forholdsmæssigt med mavevolumenet. Disse distensionssignaler kommer gennem vago -nerven i kernen i den ensomme kanal (NTS) og i dessert (AP) -området i hjerne bagagerummet. Disse oplysninger når hypothalamus og til sidst i cortex (hvor opfattelsen af distension finder sted).
Når fødevarer når maven og tarmene, frigiver disse organer forskellige peptidhormoner. Disse peptider kunne stimulere sensoriske fibre ved at tilvejebringe hjernen relateret til mængden af indtaget kalorier.
Intestinal peptid cholecistocinin (CCK) er det bedst kendte eksempel på disse signaler genereret af den samme spisning, og som kontrollerer mængden af mad, vi spiser.
Når fordøjelsen udføres, indføres mad i tolvfingertarmen, hvor det blandes med galde- og bugspytkirtelenzymer. Duodenum styrer mavetømningshastigheden gennem CCK -sekretion. Når receptorer for tolvfingertarmenvæggene registrerer tilstedeværelsen af fedt, er CCK adskilt, der giver et hæmmende signal om maven, der tømmes til tolvfingertarmen.
Men CCK har ikke kun en perifer virkning ved at kontrollere tømningen af maven, men virker på receptorer, der er placeret i de afferente fibre i vago nerven, bærer information til hjerne bagagerummet. I hjerne bagagerummet er disse Sinaptan -sensoriske fibre med neuroner, der kontrollerer refleksioner og fordøjelsesresponser.
Det antages, at aktiviteten af vago nerven produceret af CCK er synligt.
Når vagusnerven (vagotomi) er såret, eller projektionsområderne i hjerne bagagerummet er skadet, mindsker mavedistensionens kapacitet og af CCK for hæmmende indsugningsadfærd.
Leveren giver også metthedssignaler.
Administrationen af glukose i abdominalhulen (som fanges af leveren og forvandles til glycogen) reducerer indtagelsen ved at sende signaler til hjernen gennem vagusnerven.
Lange -term metthedssignaler
Det er vist, at kontrollen med indtagelsen er relateret til vedligeholdelse af kropsvægt. De fleste pattedyr har en tendens til at opretholde deres stabile vægt, Selvom der kan være en vis variation i mængden af energi, der forbruges og bruges.
Efter en periode med berøvelse og derfor af vægttab spiser dyr mere, indtil niveauerne af adipositet kommer sig.
Der er to forbindelser, der kunne defineres som "fedtsignaler" i blod, leptin (fedtvævshormon) og insulin (pancreashormon).
Leptinfunktion
Leptin er et hormon, der udskilles af fedtceller i direkte forhold til mængden af gemt fedt.
En slank individuel hemmelighed mindre leptin og en tyk hemmelighed mere. På samme måde, når en person taber vægt, falder plasma -leptinniveauer.
Betydningen af leptin som et tegn på cirkulerende fedthed i blod blev afsløret, da Zhang et al leptin). Undersøgelsen af OB / OB / mus har også været vigtig. OB / OB -mus syntetiseres ikke leptin på grund af en mutation i OB -genet. Disse dyr er kendetegnet ved at præsentere ekstrem hyperfagi og fedme. Når små mængder leptin administreres til disse dyr, normaliseres deres kropsvægt og fødeindtag.
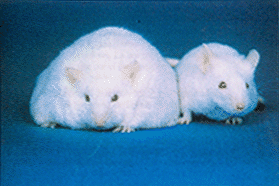
OB / OB / OB og kontrolmus. Kilde: John PJ Pinel (2001). Biopsykologi. Madrid: Prentice Hall.
Disse resultater viser, at leptin udgør et kritisk signal til kontrol af mad og vægtindtag.
Under normale forhold korrelerer mængden af leptin frigivet af fedtvæv i blodet med mængden af kropsfedt.
Den relative vægtstabilitet kunne forklares med virkningerne af leptin, Leptin øger allerede energiforbruget, indtagelse aftager.
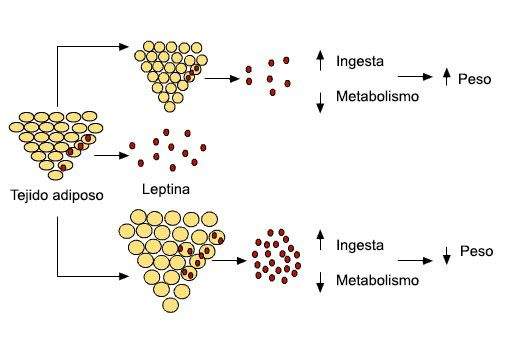
Forholdet mellem mængden af fedt, der er gemt i fedtvævet, frigivelse af leptin og kropsvægt.
Leptin fungerer ikke kun som et antiobesitetshormon, men det ser ud til at fungere som en indikator for individets individ, der informerer om energireserver er tilstrækkelige eller ikke, eller om der er en ubalance mellem bidraget og energiforbruget. Det kan også være involveret i adfærd som spilleren, der repræsenterer stort energiforbrug, og at det fra et adaptivt synspunkt kun bør implementeres under de forhold, hvor individets overlevelse er garanteret.
Leptin kan være en vigtig faktor for individets overlevelse, fungerer som et generisk informativt tegn for at fremme og bevare overlevelse.
Hvor handler den frigjorte leptin?
Vi har receptorer til leptin i hjernen (især i hypothalamus), adenohypophysis, meninges, lever, lunger, tynd tarm, gonader, fedtvæv osv. Leptin virker både i perifere væv og i centralnervesystemet.
Virkningerne af leptin på indsugningsadfærd og stofskifte er relateret til dens handling i hypothalamus.
 Frontotemporal demens, hvad er det?
Frontotemporal demens, hvad er det? Insulinfunktion
Insulin er hormonet, der gør det muligt for væv at bruge cirkulerende glukose i blod.
Insulinsekretion er direkte relateret til fedtniveauer.
Forskellige data viser betydningen af insulin som et tegn på fedthed i hjernen:
- Dyr med insulinunderskud har hyperfagi. Denne hyperfagi forsvinder, når insulin styres direkte til hjernen.
- Insulinantistofferadministration direkte til hjernen hos normale dyr øger indtagelsen.
Sammenfattende er de to hormoner, insulin og leptin tegn relateret til fedthed, der giver afferent information til hjernen. Begge hormoner frigøres i blod, og af et transportsystem i endotelcellerne i hjernekapillærerne når CNS, hvor de handler på centre, der er relateret til kontrol af energihomeostase.
- Insulin og leptin er adskilt i forhold til det lagrede fedtindhold.
- Disse hormoner fungerer i hypothalamus -stimulerende kataboliske kredsløb (de fremmer energiudgifter og hæmmer appetitten) og hæmmer anabolske kredsløb (de stimulerer indtagelse og hæmmer energiudgifter).
- Kataboliske og anabolske kredsløb har modsatte effekter på energibalancen (forskel mellem kalorier, der forbruges og slidt energi), der bestemmer mængden af lagrede fedt.
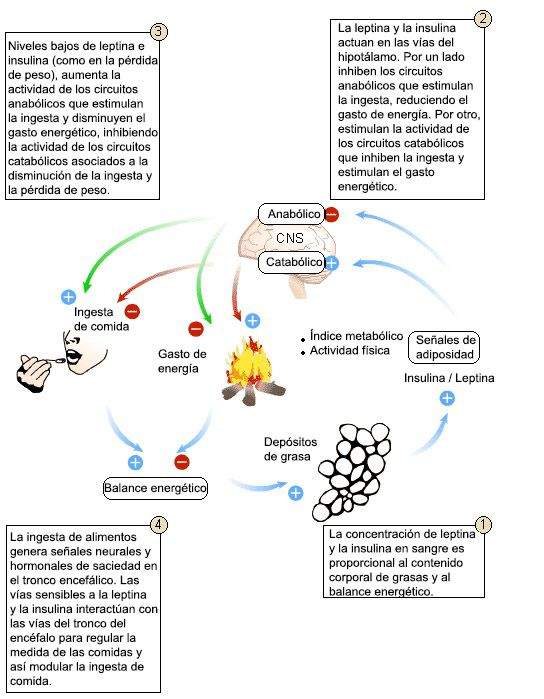
Denne model viser, hvordan ændringer i kropsfedthed er forbundet med kompenserende ændringer i fødeindtagelsen. Leptin og insulin er tegn på fedthed (udskilt i forhold til indholdet af kropsfedt), der virker i hypothalamus og stimulerer de kataboliske efferente veje og hæmmer anabolsk. Disse ruter har modsatte effekter på energibalancen (forskelle mellem kalorier, der forbruges og brugte energi), der bestemmer mængden af energi, der er gemt i form af fedt.
- « Gestalt -terapi og familiekonstellationer
- Tillid til Pareja Franqueza, oprigtighed og forståelse »

